Kapsel är en av de uråldriga doseringsformerna av läkemedel, som har sitt ursprung i det gamla Egypten [1].De Pauli, en apotekare i Wien, nämnde i sin resedagbok 1730 att ovala kapslar användes för att dölja den dåliga lukten av droger för att minska smärtan hos patienter [2].Mer än 100 år senare erhöll farmaceuter Joseph Gerard Auguste dublanc och Francois Achille Barnabe motors patentet på världens första gelatinkapsel 1843 och förbättrade den kontinuerligt för att anpassa sig till industriell produktion [3,4];Sedan dess har många patent på ihåliga kapslar fötts.År 1931 designade och tillverkade Arthur Colton från Parke Davis företaget framgångsrikt den automatiska produktionsutrustningen för ihåliga kapslar och producerade världens första maskintillverkade ihåliga kapsel.Intressant nog har tillverkningslinjen för ihåliga kapslar hittills endast kontinuerligt förbättrats på basis av Arthurs design för att förbättra produktkvaliteten och produktionseffektiviteten.
För närvarande har kapseln gjort stor och snabb utveckling inom hälso- och sjukvård och apotek, och har blivit en av de viktigaste doseringsformerna för orala fasta preparat.Från 1982 till 2000, bland de nya läkemedel som godkänts över hela världen, visade hårda kapseldoseringsformer en uppåtgående trend.
Figur 1 Sedan 1982 har nya molekylära läkemedel jämförts mellan kapslar och tabletter
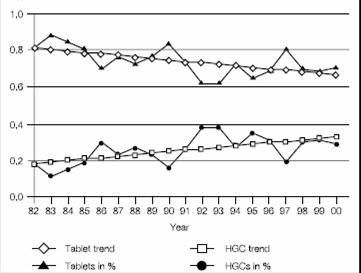
Med utvecklingen av läkemedelstillverkning och FoU-industrin har fördelarna med kapslar blivit mer erkända, främst i följande aspekter:
1. Patientpreferenser
Jämfört med andra doseringsformer kan hårda kapslar effektivt dölja den dåliga lukten av droger och är lätta att svälja.Olika färger och tryckdesigner gör droger mer igenkännbara, för att effektivt förbättra läkemedlens överensstämmelse.År 1983 visade en undersökning gjord av europeiska och amerikanska myndigheter att bland de 1000 utvalda patienterna föredrog 54 % hårda kapslar, 29 % valde sockerdragerade pellets, endast 13 % valde tabletter och ytterligare 4 % gjorde inte ett tydligt val.
2. Hög FoU-effektivitet
Rapporten från 2003 påpekade att kostnaden för forskning och utveckling av läkemedel ökade med 55 % från 1995 till 2000, och den genomsnittliga globala kostnaden för forskning och utveckling av läkemedel har nått 897 miljoner US-dollar.Som vi alla vet, ju tidigare läkemedel listas, desto längre kommer marknadsmonopolperioden för patenterade läkemedel att bli, och läkemedelsföretagens nya läkemedelsvinster kommer att öka avsevärt.Det genomsnittliga antalet hjälpämnen som användes i kapslar var 4, vilket var signifikant reducerat jämfört med 8-9 i tabletter;Testartiklarna för kapslar är också mindre, och kostnaden för metodetablering, verifiering och analys är nästan hälften så stor som för tabletter.Jämfört med tabletter är därför utvecklingstiden för kapslar minst ett halvt år kortare än för tabletter.
Generellt kan 22 % av nya sammansatta enheter inom läkemedelsforskning och -utveckling gå in i kliniska fas I-prövningar, varav mindre än 1/4 klarar kliniska fas III-prövningar.Screeningen av nya föreningar kan effektivt minska kostnaderna för nya läkemedelsforsknings- och utvecklingsinstitutioner så snart som möjligt.Därför har världens ihåliga kapseltillverkningsindustri utvecklat prekliniska kapslar (pccaps) lämpliga för gnagarförsök ®); Precisionsmikrofyllningsutrustning (xcelodose) lämplig för produktion av kliniska kapselprover ®), Och kliniska dubbelblinda kapslar (dbcaps) lämpliga för storskaliga kliniska prövningar ®) Och ett komplett utbud av produkter för att stödja Minska FoU-kostnader och förbättra FoU-effektiviteten.
Dessutom finns det mer än 9 typer av kapslar i olika storlekar, vilket ger flera val för utformningen av läkemedelsdosen.Utvecklingen av beredningsteknik och tillhörande utrustning gör också att kapseln lämpar sig för fler föreningar med speciella egenskaper, såsom föreningar olösliga i vatten.Analysen visar att 50 % av de nya sammansatta enheterna som erhålls genom screening med hög genomströmning och kombinatorisk kemi är olösliga i vatten (20%) μ G/ml), både vätskefyllda kapslar och mjuka kapslar kan tillgodose behoven hos denna sammansättningspreparat.
3. Låg produktionskostnad
Jämfört med tabletter har GMP-produktionsverkstaden för hårda kapslar fördelarna med mindre processutrustning, högt utrymmesutnyttjande, mer rimlig layout, mindre inspektionstider i produktionsprocessen, mindre kvalitetskontrollparametrar, färre operatörer, låg risk för korsföroreningar, enkel beredningsprocess, färre produktionsprocesser, enkla hjälpmaterial och låg kostnad.Enligt auktoritativa experters uppskattning är den totala kostnaden för hårda kapslar 25-30 % lägre än för tabletter [5].
Med den kraftiga utvecklingen av kapslar har ihåliga kapslar, som ett av de viktigaste hjälpämnena, också bra prestanda.Under 2007 har den totala försäljningsvolymen av ihåliga kapslar i världen överstigit 310 miljarder, varav 94 % är ihåliga gelatinkapslar, medan de övriga 6 % är från icke animaliska kapslar, varav den årliga tillväxttakten för hydroxipropylmetylcellulosa (HPMC) ) ihåliga kapslar är mer än 25 %.
Den avsevärda ökningen av försäljningen av icke animaliska ihåliga kapslar speglar konsumtionstrenden att förespråka naturliga produkter i världen.Bara i USA, till exempel, finns det 70 miljoner människor som "aldrig har ätit animaliska produkter", och 20% av den totala befolkningen är "vegetarianer".Förutom det naturliga konceptet, har icke-djurbaserade ihåliga kapslar också sina egna unika tekniska egenskaper.Till exempel har HPMC ihåliga kapslar mycket låg vattenhalt och god seghet och är lämpliga för innehåll med hygroskopicitet och vattenkänslighet;Pullulan ihåliga kapsel sönderfaller snabbt och har mycket låg syrepermeabilitet.Den är lämplig för starkt reducerande ämnen.Olika egenskaper gör olika ihåliga kapselprodukter framgångsrika på specifika marknader och produktkategorier.
REFERENSER
[1] La Wall, CH, 4000 år av farmaci, en översikt över farmaci och allierade vetenskaper, JB Lippincott Comp., Philadelphia/London/Montreal, 1940
[2] Feldhaus, FM: Zur Geschichte der Arzneikapsel.Dtsch.Apoth.-Ztg, 94 (16), 321 (1954)
[3] Französisches Patent Nr.5648, Erteilt am 25. März 1834
[4] Planche und Gueneau de Mussy, Bulletin de I'Académie Royale de Médecine, 442-443 (1837)
[5] Graham Cole, Evaluating Development and Production Costs : Tablets Versus Capsugels.Capsugel bibliotek
Posttid: maj-06-2022






